
— 新闻中心 —
冠状动脉粥样硬化血管影像学进展
7/18/18
冠状动脉造影已经广泛用于诊断冠状动脉狭窄严重程度,帮助分析罪犯血管,观察药物治疗反应,已经成为判断冠状动脉狭窄程度的金标准。但也发现冠状动脉造影显示的冠状动脉轮廓存在诸多缺陷,比如不能分析管壁病变情况。这种情况迫使发展能看清楚冠状动脉管壁的器械或系统。现有影像技术可以直接看到管壁上的斑块结构,评价再血管化术后质量,随访药物治疗效果并帮助甄别易于破裂并引起事件的高危斑块-易损斑块(vulnerable plaques), 因此血管内成像技术越来越重要。
一、计算机断层扫描(CT)
有两种不同类型的CT:电子束计算机断层摄影(EBCT:Electron beam computed tomography)和多排螺旋CT(MDCT,multi-detector-row computed tomography )。越来越多的证据表明EBCT / MDCT具有评估冠状动脉钙化(coronary artery calcification ,CAC)、冠状动脉粥样硬化和血流储备分数(FFR)的能力。
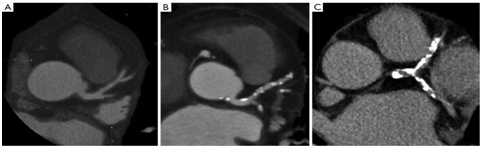

图1 MDCT冠状动脉钙化评估
(A)无任何钙化的正常冠状动脉; (B)左主干和左前降支动脉轻度钙化; (C)涉及左主干,左前降支和左回旋支的严重钙化。CAC:coronary artery calcification 冠状动脉钙化。
冠状动脉钙化通常出现在动脉粥样硬化性的晚期和高风险斑块中,呈斑点或斑点状。多项研究表明,通过CT检测的冠状动脉钙化量与组织学上的冠状动脉粥样硬化负荷相关,CAC是心血管事件的独立预测因子。没有CAC的冠状动脉事件风险只有0.5%;与低水平CAC(CAC积分=0)相比,中间水平(CAC积分100-400)CAC,相对危险度分别是4.3[95%置信区间CI,3.1-6.1], 高水平(CAC积分> 400)的CAC为7.2(95%CI,5.2-9.9,P <0.0001)。此外,CAC积分与传统Framingham风险评分相比显著增加了风险预测,特别是被认为处于中间风险的人群中(IIb推荐)。MDCT能同时评估冠状动脉钙化和狭窄,因此日渐成为主要的CT成像方式。MDCT还具有提供有关病变斑块组成信息的潜力(图2)。MDCT显示的密度与血管内超声的回声和斑块组成有着良好的对应性。MDCT的这种能力能够区分非钙化斑块,混合斑块和钙化斑块。与急性冠脉综合征相关的斑块特征包括较低的密度值、正性重塑和斑点钙化。MDCT中正性重塑和低衰减斑块的存在可预测未来的急性冠状动脉事件。

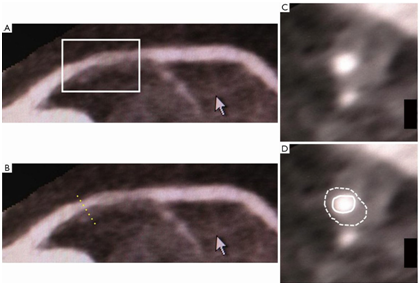
图2 通过多排螺旋CT (MDCT)评估冠状动脉斑块特征
(A)左前降支近段观察到轻度狭窄(白框); (B)该节段显示正性重塑(黄色点线); (C)具有正性重塑的节段中的横截面图像; (D)观察到显着的斑块负荷。白线,管腔面积; 白色虚线,血管壁面积。MDCT,多排螺旋CT。
这些观察结果表明在临床环境中MDCT的广泛适用性。例如,MDCT可用于筛选冠状动脉狭窄,以避免不必要的侵入性冠状动脉造影。MDCT上动脉粥样硬化斑块的高风险特征使得能够应用更强化的药物治疗以防止未来不良事件。因此,MDCT似乎适用于管理疑似或以确定冠心病的患者。
当然,MDCT也存在一定的局限性。首先,严重钙化导致的晕状伪影限制了管腔评估。在严重钙化病变的情况下,MDCT可产生假阳性结果。其次, MDCT技术有辐射暴露。此外,MDCT监测斑块组成的分辨率比侵袭性血管内成像技术差。
二、磁共振成像(MRI)和磁共振血管造影(MRA)
高分辨率MRI和MRA是冠状动脉狭窄和斑块表征的多功能非侵入性体内成像模式。最近的一项meta分析显示,MDCT在评估冠状动脉狭窄方面比MRA更准确,但MRI的特点在于能够基于生物物理和生物化学参数(如化学成分,含水量,物理状态,分子运动或扩散)区分斑块成分。MR技术的改进,如T1和T2加权、质子密度加权和飞行时间成像产生的多层增强MR(multicontrast MR)有助于分辨冠状动脉粥样硬化斑块中纤维细胞、富含脂质斑块和钙化的区域。
对比剂增强的心脏MRI对血管壁成像的可行性已经在晚期颈动脉狭窄的纤维斑块组织和新生血管中得到证明。与MDCT相比,增强心脏MRI可显示稳定的CAD患者体内主要冠状动脉中斑块组成的不同类型。在10例急性心肌梗死患者中,连续的对比增强心脏MRI成像确定了冠状动脉对比增强的空间范围及强度的变化(图3)。通过使用非对比剂T1WI MRI成像可显示斑块不稳定性(图3,图4),斑块 - 心肌信号强度比> 1.4与未来冠状动脉事件的风险增加显着相关。这些发现表明MRI在临床环境对冠状动脉粥样硬化成像的前景。但目前MRI用于冠心病诊断仍具有限制,包括成本高、检查时间长度和患者耐受程度差。预期进一步的技术进步将使MRI更加适用于临床需要。

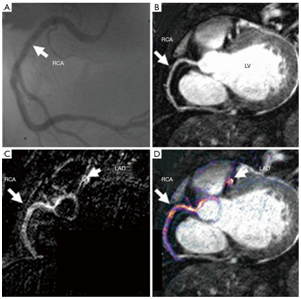
图3 冠状动脉对比剂增强的心脏MRI
(A)侵入性冠状动脉造影显示右冠状动脉存在轻度狭窄; (B)MRA显现右冠状动脉; (C,D)对比增强心脏MRI显示右冠状动脉中的弥漫性对比增强(白色箭头)。MRI,磁共振成像; MRA,磁共振血管造影。

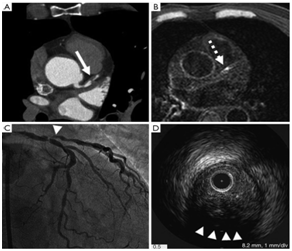
图4 MRI上的HIP测量
(A)MDCT确定在左前支近端具有正性重塑的狭窄(箭头); (B)在CMR的相应区段观察到“高信号点”(虚线箭头)(C)侵入性冠状动脉造影显示在左前降支近端(箭头)处的严重冠状动脉狭窄; (D)IVUS成像中观察到的正性重塑和超声衰减(箭头)。IVUS,血管内超声; HIP,高信号斑块; MDCT,多检测器行计算机断层扫描。CMR,冠状动脉MR。
三、灰阶血管内超声(grayscale IVUS)
IVUS (intravascular ultrasound,IVUS)应用微晶体元件,可产生高分辨率的横切血管壁和管腔图像。纵向分辨率(Axial resolution)约150μm,横向分辨率(lateral resolution)约300μm。可以定量分析管腔、管壁和斑块面积。IVUS指导下的PCI(percutaneous coronary intervention ,PCI)能减少再狭窄率、支架血栓和血栓事件11。还可以用于观察药物治疗后冠状动脉斑块的自然发展。
灰度IVUS将斑块分为4型。软斑块:病变的超声反射性低于周边的外膜;纤维斑块:超声反射性位于软斑块和钙化斑块之间。钙化斑块:具有比外膜更强的超声反射性并伴有声影。混合斑块:具有多种超声反射特征。IVUS还能分辨更多的超声特点斑块(图5)。灰阶IVUS是一种侵入性方法,需要在冠状动脉造影时才能完成,对动脉粥样硬化斑块成份的构成特征显示不够理想。

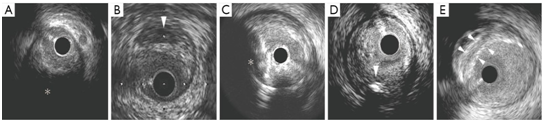
图5 灰阶IVUS 斑块形态(IVUS, intravascular ultrasound)
(A) 低回声斑块(Attenuated plaque): 3-9点钟(星号标识); 伴有深超声衰减(deep ultrasound attenuation)的低回声斑块(Attenuated plaque),没有钙化,或者是非常致密的纤维斑块(图5A)。组织学上低回声斑块含有坏死核心或者病理学上内膜增厚(pathological intimal thickening ,PIT)和大脂质核心。ACS的罪犯血管常常可见低回声斑块,PCI围手术期容易发生心肌梗死和慢血流。
(B) 无回声斑块(echolucent plaque): 箭头示斑块内无回声区; 无回声斑块指斑块内缺乏超声反射或低超声反射(图5B),斑块内含有较高的脂质,坏死核心相对小,与衰减斑块比较脂质池也比较小,是急性心肌梗死患者罪犯病变的特征性标志。
(C) 钙化结节(calcified nodule): 不规则内腔表面并突出腔内;钙化结节也是冠状动脉急性事件的斑块类型。主要为纤维钙化斑块,很少或没有坏死核心,致密钙化的结节使管腔表面不光滑或突出血管腔,表面可见血栓覆盖,PROSCPET 研究发现钙化结节很少发展为ACS事件。
(D) 点状钙化(spotty calcification): 斑块内小钙化点;严重钙化临床上比较稳定,星罗棋布或点状钙化斑块多不稳定。病理学研究显示高危病变内的小量钙化常常会引起ACS 或猝死。点状钙化的特征是斑块内仅含有少量钙化,钙化弧度小于90度,常常会加快斑块进展,斑块易变,疾病发展迅速。
(E) 多层斑块(multiple layer appearance):多个箭头标识处。在灰阶IVUS超声显示的多层斑块是冠心病患者的高危特征。提示反复发生附壁血栓,与斑块进展有关。
四、虚拟组织学血管内超声(Virtual histology intravascular ultrasound ,VH-IVUS)
灰介IVUS对动脉粥样斑块内组织成份的分析能力是有限的。VH-IVUS则能进一步分析斑块内组织成分,把超声的射频反射能量变成颜色编码的肉眼可视的彩色组织地图,它把斑块分为: 纤维斑块(fibrous),纤维脂肪斑块( fibrofatty),坏死核心斑块( necrotic core) 和致密钙化斑块(dense calcium);尸检准确率分别为 79.7%, 81.2%, 85.5%, 92.8%。吣?7岁,10年(2006年)前植入金属裸支架。2017年OCT显示:A.内膜弥漫增厚,4-6点胆固醇结晶斑块,表面可见纤维帽;B.支架表面内膜弥漫增厚,13-15点内膜增厚处,可见内膜不规则,内膜下可见脂质池(新生动脉粥样硬化斑块)
OCT局限性在于OCT组织穿透性差,只有2-3mm,内弹力膜以外的组织很难成像,并容易受血液的干扰。由于穿透力差,很难评价完整的斑块,也不适合于观察大直径动脉的动脉粥样硬化斑块。红外线不能穿透红细胞,OCT成像过程中,需要对比剂注射。
七、近红外线光谱镜(Near-infrared spectroscopy ,NIRS)
光谱镜是利用光与分子的相互作用,测量电磁谱。在冠状动脉腔内,由于生物组织的不同化学特征,NIRS图像可以分析动脉粥样硬化斑块内的脂质和蛋白含量。NIRS探测脂质成份的敏感性和特异性分别为90% 和 93% 。导管NIRS成像系统已经用于临床(InfraReDx, Burlington, Massachusetts, USA)。也称为化学成像(chemogram)(图9)。
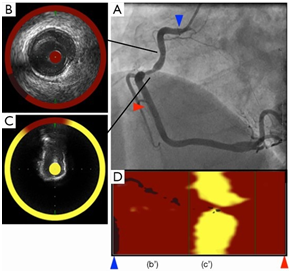

图9 NIRS-IVUS探测的右冠状动脉脂质斑块
A.导管从右冠状动脉的中段(红箭头)自动回抽到右冠状动脉近端(蓝箭头)。B.IVUS 显示9-4点钟可见斑块。IVUS图像周围的环代表NIRS值。脂质斑块呈黄色,非脂质斑块呈红色。在这个病变中,NIRS值提示斑块为非脂质斑块。C.右冠状动脉中段IVUS横切面图像显示表面钙化和钙化后无回声阴影。NIRS值显示近环形脂质斑块。D.该图显示红箭头和蓝箭头之间的右冠状动脉化学成像。b’对应图5B病变;c’对应图5C;NIRS: near infrared spectroscopy; IVUS:intravascular ultrasound。
NIRS值可确定高危斑块。研究发现罪犯血管常常伴有大的脂质负荷指数(LCBI: lipid core burden index);LCBI大于400,提示STEMI患者罪犯斑块含有大量脂质负荷斑块,是一个理想的LCBI分界值。如果结合NIRS 和灰阶IVUS能更好的评价斑块特征。NIRS 测的LCBI结合灰阶超声获得的斑块负荷能明显提高纤维动脉粥样硬化斑块的探测准确性。LCBI > 500 容易发生PCI术后心肌梗死。 这些结果提示LCBI未来可用于冠状动脉事件的分层和PCI 预后评价。NIRS 成像系统缺陷在于NIRS 不能评估脂质核心的深度和脂质定量。现有的NIRS 成像系统也不能评估纤维帽和巨噬细胞。
八、冠状动脉血管镜
冠状动脉血管镜(Intracoronary coronary angioscopy)通过纤维光学系统可以斑块的表面,体内分标率<150 μm。冠状动脉血管镜的优点是分析斑块颜色和斑块表面特征。斑块的颜色分级为:白、浅黄、黄和深黄(图10)。白色:纤维斑块;黄色:富脂质或坏死核心斑块;深黄色:不稳定斑块,伴有薄纤维帽和大脂质核心。稳定的斑块,表面光滑;复杂的斑块表面不规则;血管镜还可以看到破溃斑块、虫蚀斑块、纤维帽、裂缝斑块和溃疡斑块。血栓的镜下特征为:红色、白色或混合团块,团块与内膜相连或突出于管腔。灰阶IVUS探测血栓的敏感度57%,血管镜探测血栓的敏感度为100%。血管镜局限性包括:不能定量分析斑块;只能看到管腔内斑块的表面;需要持续注射盐水置换冠状动脉内的血液影响。

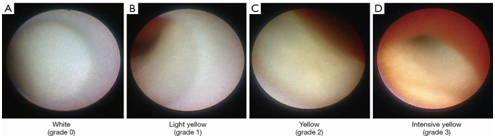
图6 血管镜斑块分类
grade 0 = 白色(white); grade 1 =浅黄( light yellow); grade 2 = 黄色(yellow); grade 3 = 深黄(intensive yellow)
表 1 不同血管内成像系统的功能特点


九、总结和展望
现有侵入性体内成像系统可以评估斑块负荷和斑块成份、确定易损斑块、帮助探讨与冠状动脉事件相关的动脉粥样硬化机制和追踪抗动脉硬化药物对冠状动脉硬化的影响。这些器械大大推动了我们对冠状动脉粥样硬化的了解,但是这些器械的轴向分辨率、穿透性和区分斑块成分的能力依然有限(表1)。如果能提高空间分辨率,就能进一步准确分析冠状动脉粥样斑的构成。新一代OCT分辨率约为10 μm ,可以清晰分析细胞和亚细胞结构。影像融合技术有可能克服每种成像系统的内在限制。例如:NIRS和IVUS融合可以同时评估血管结构和斑块成份。正在研制的新的融合成像系统有希望实现神奇的斑块成像,帮助临床医生理解和观察斑块并更有效地用于处理冠心病患者。


